PCM ve stavebnictví Díl 1: Základní charakteristiky PCM
Článek seznamuje čtenáře se základními požadavky na vlastnosti materiálů využívajících fázové přeměny ve stavebnictví. Tyto látky bývají označovány jako PCM. Dále se článek zabývá možným chemickým složením PCM, výhodami a nevýhodami jednotlivých fázových přechodů.
K sepsání seriálu článků pojednávajících o využití PCM ve stavebnictví mě motivovalo množství dotazů obracejících se na moji osobu ohledně této problematiky na základě mé diplomové práce Využití materiálů s látkovou přeměnou (PCM) ve stavebnictví. V seriálu článků bych chtěla čtenáře seznámit s možnostmi, výhodami a nevýhodami, které aplikace těchto materiálů v budově poskytuje, při použití ať už jako stavební prvek nebo jako součást systému TZB.
V dnešním prvním díle bych se chtěla zaobírat základními charakteristikami a principy použití těchto látek. Proto tento článek obsahuje více teoretických informací než díly následující, které budou zaměřeny na konkrétní produkty a aplikace.
Z historie
Mezi materiály, které se řadí do kategorie těch, které při správném použití mohou snížit potřebu energií na vytápění a na chlazení, patří i tzv. Phase Change Materials (materiály s látkovou přeměnou). Tyto materiály jsou ve světové literatuře označovány zkráceně jako PCM. Nejedná se o žádnou převratnou novinku, vždyť první použití PCM technologií jsou známy už od 20. a 30. letech 20. století.
Například už v roce 1932 bylo prvně patentováno zařízení pro ohřev teplé vody s pomocí akumulátoru s PCM. Známé jsou i aplikace ve vesmírných lodích, jejichž výzkum probíhal na základě zadání Úřadu pro letectví a kosmonautiku ve Spojených státech amerických (NASA). V roce 1965 byly patentovány ohřívací vložky s hydridem lithia pro horolezce, polární badatele a letce. V potravinářském průmyslu je využití skupenské přeměny látek již mnoho desítek let na denním pořádku.
Pro uplatnění PCM ve stavebnictví byl průlomový rok 1946, kdy byla nedaleko Bostonu (USA) vystavěna na tuto dobu nevídaná budova tzv. Dover House. Stavba obsahovala prostory, jejichž stěny působily jako radiátory do sousedních místností. V těchto prostorách byly umístěny plastové sudy s náplní Glauberovy soli (celkem 21 tun), které byly ohřívány důmyslným systémem využívajícím sluneční energie. Tyto prostory měly akumulační potenciál až 11 MJ (3 kWh).
Aplikace PCM v ƒåesk√© republice souƒçasn√© dobƒõ ponƒõkud pokulh√°v√° za st√°ty Z√°padn√≠ Evropy (p≈ôedev≈°√≠m Nƒõmecko, ≈Ýv√Ωcarsko a Francie), USA a Japonskem. V ƒçesk√© odborn√© literatu≈ôe se setk√°v√°me sp√≠≈°e se st≈ô√≠pky informac√≠ o PCM. Jedn√° se p≈ôedev≈°√≠m o ƒçl√°nky popisuj√≠c√≠ nov√© produkty zahraniƒçn√≠ch v√Ωrobc≈Ø ƒçi popis aplikace v zahraniƒç√≠.
Látková přeměna a latentní teplo
Prvně si ujasněme základní pojmy související s fázovou přeměnou látky. Při změně skupenství z kapalného stavu na pevné skupenství hovoříme o krystalizaci (např. zamrzání vody). Opačný děj, kdy se pevné skupenství mění na kapalné, nazýváme tání. Tyto fázové/látkové přeměny se uskutečňují pro daný materiál za konstantní teploty. Proces krystalizace a tání má pouze omezený počet opakování (cyklů), kdy se nemění fyzikální a chemické vlastnosti látky. Mezi latentní změny patří samozřejmě i další změny skupenství např. plyn-kapalina (kondenzace) nebo pevné skupenství-plyn (sublimace), tyto druhy fázových přeměn ovšem PCM materiály nevyužívají. Latentní teplo je poměrně velké množství energie, které je potřeba v průběhu fázové přeměny vydat anebo pohltit. Právě toto teplo odlišuje PCM od ostatních materiálů, které využívají pouze citelného tepla.
Citelné teplo běžného stavebního materiálu:
![]()
Citelné a latentní teplo materiálu s PCM:
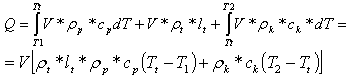
Následující příklad jednoduchou cestou představuje základní výhodu použití PCM, a to je využití latentního tepla. Je třeba upozornit, že hlavním požadavkem na plné využití tohoto fenoménu je vhodná volba teplotního rozmezí v závislosti na teplotě tání PCM.
Příklad
Kolik energie naakumuluje 1m3 parafínu s teplotou tání 23 °C - 25 °C a latentním teplem 70 kJ/kg při teplotě 15-30 °C:
Citelné teplo:
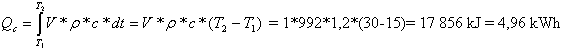
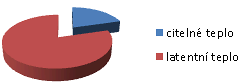
Latentní teplo:
![]()
Celkovƒõ: Qtot = 24,24 kWh
Pozn. Při výpočtu uvažuji shodnou hodnotu měrné tepelné kapacity pro pevnou i kapalnou fázi.
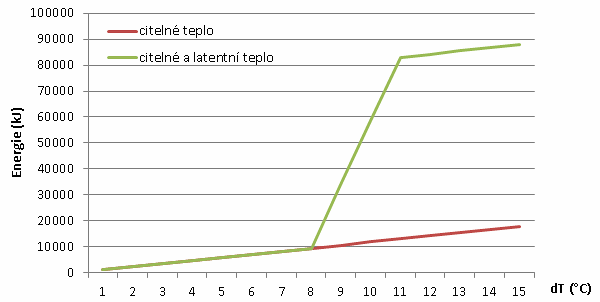
Grafické porovnání naakumulované energie při využití latentního tepla a bez
| Přechod skupenství | Objemové změny | Latentní teplo | Další vlastnosti a poznámky | |
|---|---|---|---|---|
| Pevné | Pevné | Malé | Malé | Jedná se o změnu krystalizační struktury. Vhodné např. pro Trombeho stěny. Př. Pentaglycerin-bod tání 81 °C, latentní teplo tavení 216 kJ/kg |
| Pevné | Plynné | Velké | Velké | Kvůli obrovským objemovým změnám nepoužitelné |
| Kapalné | Plynné | Velké | Velké | Kvůli obrovským objemovým změnám nepoužitelné |
| Pevné | Kapalné | Malé | Střední | Objemová změna dosahuje maximálně 10 %. PCM nelze využít jako teplonosnou látku. |
Výhody a nevýhody jednotlivých fázových přechodů
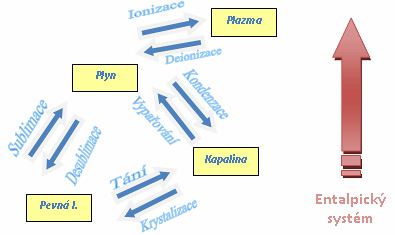
Látkové přeměny a jejich entalpická hladina
Z výše uvedeného vyplývá, že ačkoliv je entalpická hladina pevné a kapalné fáze poměrně nízká (v porovnání s jinými skupenstvími), rozhodujícím faktorem při výběru vhodných materiálů využívajících fázové změny ve stavebnictví jsou objemové změny.
Základní charakteristiky
Základní požadavky na PCM
- Neho≈ôlavost
- Netoxick√Ω materi√°l
- Chemick√° stabilita
- Vysoké měrné skupenské teplo fázového přechodu
- Vysok√° tepeln√° kapacita
- Recyklovatelnost
- Odolnost proti "supercooling"
- P≈ôijateln√° cena
Vlastnosti PCM
- Teplotně-fyzikální vlastnosti
- Kinetické vlastnosti
- Chemické vlastnosti
- Ekonomické vlastnosti
Teplotně-fyzikální vlastnosti
- Teplota tání v potřebném rozmezí
- Velké latentní teplo tání
- Vysok√° tepeln√° kapacita
- Vysoká tepelná vodivost v obou skupenstvích
- Malé objemové změny
- Nízký tlak tvořících se par
- Stálost vlastností
Kinetické vlastnosti
- Vysoká nukleace zabraňující přechlazení (jádra potřebná k vytvoření krystalizačních zárodků)
- Vysoká rychlost růstu krystalů
Chemické vlastnosti
- Absolutně vratný cyklus krystalizace a tání
- Stálost vlastností i s rostoucím počtem cyklů
- Nesmí být korozivní ve vztahu k ostatním materiálům
- Netoxický, nezápalný nevýbušný
Ekonomické vlastnosti
- Dostupn√Ω
- Nákladově efektivní
Chemické složení
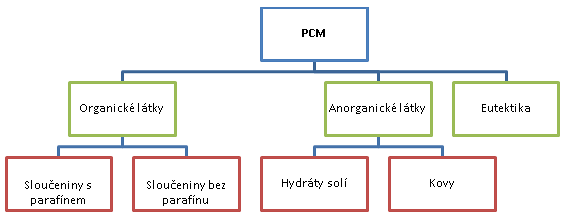
Organické látky
Tuto skupinu PCM můžeme dělit na sloučeniny s parafíny a na sloučeniny bez parafínů. Velkou výhodou těchto sloučenin je jejich vlastní nukleace. Díky této vlastnosti téměř nedochází k problémům s přechlazováním.
Sloučeniny s parafíny
Parafin je směs pevných uhlovodíků řady CnH2n+2. Pro použití v TZB se využívá téměř přímý řetězec CH3-(CH2)-CH3. Pro krystalizaci řady (CH3) je nutné velké množství latentního tepla. Právě díky této vlastnosti jsou tyto sloučeniny velmi vhodné pro použití jako PCM. Další kladnou vlastností parafínů je jejich chemické inertnost a cenová dostupnost. Tyto materiály mají poměrně dlouhý cyklus krystalizace-tání.
Sloučeniny bez parafínů
Tato kategorie obsahuje velké množství organických látek s rozdílnými vlastnostmi. Tvoří tak velkou skupinu látek, které se velmi hodí k použití jako tepelný zásobník.
Do této skupiny patří estery, vyšší mastné kyseliny, glykoly apod. Problematickou vlastností je jejich hořlavost, která nedovoluje jejich styk s vyššími teplotami, plamenem a oxidačními činidly. Z ekonomického hlediska jsou nevýhodné, protože jsou velmi drahé. Jejich cena se pohybuje dvou až tří násobně výš než u technických parafínů.
Další vlastnosti:
- Vysoké teplo tání
- Ho≈ôlavost
- Nízká teplotní vodivost
- Nízká zápalná teplota
- Toxicita- hodnota se velmi mění pro každou látku
- Nestabilita p≈ôi vysok√Ωch teplot√°ch
V následující tabulce vybírám organické látky s nejslibnějšími charakteristikami pro použití v tepelných zásobnících. A.Sharma ve své práci Renewable and Sustainable Energy Reviews 13 (2009) označuje tuto skupinu jako kategorii I.
| Kategorie P/NP/MK | Název | Teplota tání (°C) |
Latentní teplo tání (kJ/kg) | |
|---|---|---|---|---|
| P | Počet atomů uhlíku | 14 | 5.5 | 228 |
| P | 16 | 16.7 | 237.1 | |
| P | 20 | 36.7 | 246 | |
| NP | D-kyselina mléčná | 26 | 184 | |
| Trimyristin | 33-57 | 201-213 | ||
| MK | Kyselina octov√° | 16.7 | 184 | |
| MK | Polyetylen glykol 600 | 20-25 | 146 | |
| MK | Kyselina palmitov√° | 55 | 163 | |
| MK | Kyselina myristov√° | 58 | 199 | |
Pozn. P-sloučeniny s parafíny, NP- sloučeniny bez parafínů, MK-mastné kyseliny
Anorganické látky
Do skupiny anorganický látek můžeme zahrnout hydráty solí a kovy.
Hydráty solí
"Hydr√°ty sol√≠ jsou l√°tky, kter√© ve sv√© struktu≈ôe obsahuj√≠ v√°zan√© (komplexnƒõ i hydrataƒçnƒõ) molekuly vody. Zah≈ô√≠v√°n√≠m se tyto molekuly vody od≈°tƒõpuj√≠ a rozpou≈°tƒõn√≠m l√°tek ve vodƒõ opƒõt poutaj√≠ molekuly vody. P≈ôi pout√°n√≠ molekul vody - hydrataci - se u nƒõkter√Ωch slouƒçenin uvol≈àuje tzv. hydrataƒçn√≠ teplo - nap≈ô. CaCl2 + 2 H2O → CaCl2 . 2H2O + teplo."
Lze je zapsat obecným vzorcem AB*nH2O. Proces tání je ve skutečnosti dehydratace. Hydráty solí většinou tají buď do:
- hydr√°t≈Ø s men≈°√≠m poƒçtem molekul vody: AB*nH2O → AB*mH2O+ (n-m)H2O
- nebo do bezvod√© formy: AB*nH2O → AB + nH2O
To znamená, že při změně skupenství z pevného na kapalné se hydráty rozpadnou do anhydrátu soli a vody nebo do hydrátu nižšího řádu a vody. To u většiny hydrátů vyvolává zásadní problém. Nekongruentní tání způsobuje, že menší množství molekul vody již není schopné roztavit všechny pevné látky. Ty se díky větší hustotě začnou propadat na dno. Tím se snižuje množství látek, které mění skupenství a tedy i celkové pohlcené/uvolněné latentní teplo.
Dalším nedostatkem hydrátů solí je fakt, že nemají dostatek nukleačních činitelů, proto je potřeba tyto činitele dodávat tak, aby nedocházelo k přechlazování tzv. supercoolingu.
Pro lepší funkci hydrátů solí se obecně doporučuje:
- mechanické míchání,
- zapouzdření do kapslí,
- přidání zahušťovadel, která zabrání sedání solí na dno,
- napojení zásobníku na přívod vody.
Kovy
Kovy jsou skupinou PCM, která zatím čeká na své výraznější uplatnění. Jejich největším problémem je objemová hmotnost. Například Gallium, prvek, který taje při 29.7 °C má hustotu 5 910 kg/m3. Tyto látky oplývají vysokým latentním teplem na jednotku objemu, ale velmi nízkou latentní teplotou na kg (Ga- 80 kJ/kg).
Eutektické materiály
"Eutektikum je tuhá směs dvou látek, jejichž krystaly se vytváří při tuhnutí společně. Čisté eutektikum vzniká v takovém mísícím poměru obou složek, při kterém je teplota tuhnutí směsi nejnižší. Pokud je mísící poměr odlišný, vzniká směs podeutektická, u které je tuhá fáze tvořena směsí eutektika a krystalů jedné složky, nebo směs nadeutektická, u které je tuhá fáze tvořena směsí eutektika a krystalů druhé složky."
Eutektické směsi voda-sůl mají velmi podobnou tepelnou vodivost jako samotná voda. Výhodou eutektik je jejich chemická stabilita. Jednou z nevýhod při použití těchto směsí jsou především korozivní vlastnosti. Objemová změna je během tání a krystalizace okolo 5 - 10 %.
| Materiál | Teplota tání [°C] | Latentní teplo [kJ.kg-1] | Hustota pevný [kg.m-3] | Hustota kap. [kg.m-3] |
|---|---|---|---|---|
| KCl (19.5 wt.%)/H2O | -10.7 | 283 | 1 126 | 1 105 |
| NaCl (22.4 wt.%)/ H2O | -21.2 | 222 | 1 165 | 1 108 |
| Al(NO3)3 (30.5 wt.%)/ H2O | -30.6 | 131 | 1 283 | 1 251 |
Eutektické směsi voda-sůl
| Materiál | Kompozice [%] | Teplota tání [°C] | Latentní teplo [kJ.kg-1] |
|---|---|---|---|
| Mg(NO3)3*6H2O + NH4NO3 | 40-60 | 30 | 200.5 |
| Mg(NO3)3*6H2O + MgCl2*6H2O | 61.5-38.5 | 52 | 125.5 |
| Mg(NO3)2*6H2O + MgBr2*6H2O | 59-41 | 66 | 168 |
Organické a anorganické eutektika (podle A.Sharmy kategorie I.)
V√Ωroba PCM
Následující kapitola popisuje postup při výrobě PCM. Pro demonstraci jsem vybrala produkci parafínových mikrokapslí od společnosti BASF.
Postup v√Ωroby
V prvním kroku je smíchána vosková emulze s detergenty. Během celého procesu je směs neustále promíchávána. Dále se do směsi vloží monomery a startovací látky. Na rozhraní vody a vosku tak začne docházet k růstu polymerové vrstvy, která později vytvoří nepropustný a velmi odolný obal pro jednotlivé kapičky vosku. Celá směs v konečné fázi obsahuje 42 % pevných látek.
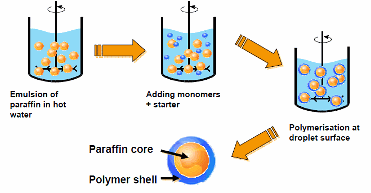
Schematický postup při výrobě mikrokapslí společnosti BASF
(zdroj energiforumdanmark.dk)

Finální výrobek-tekutá disperze vlevo, dále prášek a detail mikrokapsle skládající se z voskového jádra a polymerního obalu.
(zdroj energiforumdanmark.dk)
Z√°vƒõr
Z dnešního dílu, představujícího základní principy a materiály použitelné jako PCM, lze usoudit, že potencionálních PCM je velké množství. Příští díl již ukáže, které typy PCM jsou v praxi konkurence schopné běžným materiálům. Tento díl již bude zaměřen na konkrétní produkty, které lze zakoupit v ČR nebo v ostatních státech Evropy a použít jako stavební prvek.
Použitá literatura:
HEJHÁLEK, J.: Stálá teplota v létě pomocí technologie PCM. Stavebnictví a interiér, 2006, c. 9, s. 50-52.
VERNER, Carl. PHASE CHANGE THERMAL ENERGY STORAGE. 1997. The Department of The Built Environment: University of Brighton, 1997. 105 s. Dostupné z WWW.
ZAVORALOVÁ, Pavla. Využití materiálů s fázovou přeměnou (PCM) ve stavebnictví. [s.l.], 2010. 120 s. Diplomová práce. České vysoké učení technické v Praze, Fakulta stavební, Katedra technických zařízení budov.
TYAGI, Vineet; BUDHI, D. PCM thermal storage in buildings : A state of art. In . India : Elsevier, 2005. s. 50-53.
SHARMA, A; TYAGI, V.V.; CHEN, C.R.; BUDDHI, D. Review on thermal energy storage with phase changenext term materials and applications . In SHARMA, Atul. Renewable and Sustainable Energy Reviews [online]. [s.l.] : Elsevier, February 2009 [cit. 2010-11-01]. Dostupné z WWW.
D.V. Hale, M.J. Hoover and M.J. O'Neill, Phase change materials hand book, Marshal Space Flight Center, Alabaa (1971).
Vodík. In Wikipedia : the free encyclopedia [online]. St. Petersburg (Florida) : Wikipedia Foundation, , last modified on 29.10.2010 [cit. 2010-11-01]. Dostupné z WWW.
Eutektikum. In Wikipedia : the free encyclopedia [online]. St. Petersburg (Florida) : Wikipedia Foundation, 7.1.2007, last modified on 5.8.2010 [cit. 2010-11-02]. Dostupné z WWW.
Mehling H., Cabeza L. F., Heat and Cold Storage with PCM, Springer, Berlín, 2008.
Energi Forum Danmark [online]. 2008 [cit. 2010-11-04]. Phase Change Material-Micronal. Dostupné z WWW.
The article introduces the basic requirements for properties of materials using phase change in construction. These substances are known as PCM. Furthermore, the article deals with the possible chemical composition of the PCM, the advantages and disadvantages of phase transitions.