MikrobiĂĄlnĂ mikroklima budov (II)
SbÄr a kultivace vzorkĆŻ z rodinnĂœch domĆŻ
Tento dĂl se zamÄĆuje na problematiku sbÄru vzorkĆŻ pro analĂœzu mikrobiĂĄlnĂ kontaminace prostĆedĂ v rodinnĂœch domech v okolĂ Brna. CĂlem bylo vytipovat vhodnĂ© metody, kterĂ© jsou v praxi pouĆŸitelnĂ©, pĆimÄĆenÄ nĂĄkladnĂ© a dobĆe popisujĂ stav kontaminace prostĆedĂ, aby bylo moĆŸno nejen zhodnotit kvalitu vzduchu, ale takĂ© hledat pĆĂÄiny zjiĆĄtÄnĂ©ho stavu. Ć etĆenĂ bylo provedeno v domech vybavenĂœch vzduchotechnikou a pro porovnĂĄnĂ takĂ© v domech s pĆirozenĂœm vÄtrĂĄnĂm.
1 Ăvod
V prvnĂm dĂle byla obecnÄ pĆedstavena problematika mikrobiĂĄlnĂho mikroklimatu budov a takĂ© skuteÄnost, ĆŸe v ÄeskĂ© republice platĂ zĂĄvaznĂĄ vyhlĂĄĆĄka pro pobytovĂ© mĂstnosti staveb [1], kterĂĄ pĆedepisuje, ĆŸe v pobytovĂœch mĂstnostech (veĆejnĂœch staveb, ale hygienickĂĄ pravidla majĂ jistÄ obecnou platnost) je nepĆĂpustnĂœ viditelnĂœ nĂĄrĆŻst plĂsnĂ na zdech a povrĆĄĂch. Za prokĂĄzanĂœ rĆŻst plĂsnĂ na povrchu se ve spornĂœch pĆĂpadech povaĆŸuje i nĂĄlez potvrzenĂœ odbÄrem a kultivacĂ na ĆŸivnĂ© pĆŻdÄ – tj. i mnoĆŸstvĂ okem neviditelnĂ©, mĆŻĆŸe bĂœt hodnoceno jako zĂĄvadnĂ©. DĂĄle je pĆedepsĂĄno, ĆŸe mimo prostory vyĆŸadujĂcĂ zvĂœĆĄenĂ© nĂĄroky na Äistotu je stanovena maximĂĄlnĂ koncentrace bakteriĂ 500 KTJ (kolonie tvoĆĂcĂ jednotky)/m3 vzduchu a maximĂĄlnĂ koncentrace plĂsnĂ rovnÄĆŸ 500 KTJ/m3 vzduchu. Jak bylo uvedeno minule, tyto koncentrace korespondujĂ s celoevropskĂœm prĆŻmÄrem. PĆestoĆŸe nejsou tyto limity pĆedepsĂĄny pro bytovĂ© prostĆedĂ, z podstaty vÄci vyplĂœvĂĄ, ĆŸe v bytovĂ©m prostĆedĂ trĂĄvĂ ÄlovÄk hodnÄ Äasu a tudĂĆŸ expozice jakĂœmikoli ĆĄkodlivinami je zde dlouhodobĂĄ a ze zdravotnĂho hlediska vĂœznamnĂĄ. VĂme vĆĄak, jsou-li tyto limity splnÄny? JednĂm ze zĂĄsadnĂch technickĂœch prostĆedkĆŻ jak vytvoĆit kvalitnĂ vnitĆnĂ prostĆedĂ je nucenĂ© vÄtrĂĄnĂ vybavenĂ© filtracĂ vzduchu. PrvotnĂm dĆŻvodem pro instalaci nucenĂ©ho vÄtrĂĄnĂ v bytovĂ© vĂœstavbÄ je samozĆejmÄ Ășspora tepla pouĆŸitĂm jeho zpÄtnĂ©ho zĂskĂĄvĂĄnĂ nejÄastÄji vĂœmÄnĂkem vzduch/vzduch, ale dalĆĄĂ aspekty vzduchotechniky by nemÄly bĂœt opomĂjeny. Je vzduchotechnika pĆĂnosem, nebo naopak pĆĂtÄĆŸĂ z hlediska mikrobiĂĄlnĂ sloĆŸky vnitĆnĂho vzduchu? Pro odpovÄÄ na tuto otĂĄzku jsme provedli ĆĄetĆenĂ ve skupinÄ 10 rodinnĂœch domĆŻ na jiĆŸnĂ MoravÄ.
1.1 OkrajovĂ© podmĂnky mÄĆenĂ
![Obr. 1 – SezonnĂ vĂœkyvy koncentrace plĂsnĂ ve venkovnĂm ovzduĆĄĂ v jiĆŸnĂm Rakousku [2]](/docu/clanky/0129/012972o1.png)
Obr. 1 – SezonnĂ vĂœkyvy koncentrace plĂsnĂ ve venkovnĂm ovzduĆĄĂ v jiĆŸnĂm Rakousku [2]
OdbornĂĄ literatura uvĂĄdĂ, ĆŸe koncentrace plĂsnĂ v interiĂ©rech se pohybuje v ĆĄirokĂ©m rozmezĂ a vĂœznamnÄ se odvĂjĂ od koncentrace plĂsnĂ ve venkovnĂm vzduchu. Ve venkovnĂm ovzduĆĄĂ se plĂsnÄ vyskytujĂ zejmĂ©na v lĂ©tÄ a na podzim, kdyĆŸ je teplo a vlhko. Na obr. 1 je znĂĄzornÄna prĆŻmÄrnĂĄ hodnota, rozptyl a max. a min. hodnoty zjiĆĄtÄnĂ© bÄhem roku ve Ć tĂœrsku v jiĆŸnĂm Rakousku. PozorovĂĄnĂ z jinĂœch evropskĂœch i mimoevropskĂœch lokalit ukazujĂ, ĆŸe celosvÄtovÄ pĆevlĂĄdajĂ rody Cladosporium, Aspergillus a Penicillium a jejich ÄasovĂ© rozloĆŸenĂ je podobnĂ© [2].
Jak je vidÄt, nejlepĆĄĂ stav ovzduĆĄĂ je v zimÄ a na jaĆe, kdy nepĆĂznivĂ© nĂzkĂ© teploty brĂĄnĂ pĆeĆŸĂvĂĄnĂ spĂłr plĂsnĂ ve vzduchu. TakĂ© je vidÄt, ĆŸe splnÄnĂ limitu 500 KTJ/m3 v letnĂm obdobĂ je v budovĂĄch s pĆirozenĂœm vÄtrĂĄnĂm za bÄĆŸnĂœch vnÄjĆĄĂch podmĂnek nereĂĄlnĂ©. Z tohoto dĆŻvodu se naĆĄe ĆĄetĆenĂ odehrĂĄvalo na jaĆe, kdy je pĆirozenĂ© pozadĂ nĂzkĂ©.
DalĆĄĂ podmĂnky, kterĂ© je tĆeba pro porovnĂĄvĂĄnĂ vĂœsledkĆŻ zaznamenat, souvisĂ s polohou, velikostĂ, vybavenĂm a uĆŸĂvĂĄnĂm domu. ZĂskĂĄme tak informace o vlastnĂm prostĆedĂ, ve kterĂ©m je sbÄr provĂĄdÄn. Je nezbytnĂ© zaznamenat hodnoty, jako jsou teploty, relativnĂ vlhkosti vzduchu i povrchĆŻ, ze kterĂœch je vzorek odebĂrĂĄn, a dalĆĄĂ souvisejĂcĂ faktory, jako napĆ. pĆĂtomnost domĂĄcĂch mazlĂÄkĆŻ, Äetnost Ășklidu, zneÄiĆĄtÄnĂ oklnĂho exteriĂ©ru a dalĆĄĂ (vĂce viz [3]). PromÄnlivost vĂœskytu sledovanĂœch ĆĄkodlivin je velmi odliĆĄnĂĄ, a to nejen mezi budovami (i sousednĂmi), ale takĂ© mezi jednotlivĂœmi mĂstnosti ve stejnĂ©m domÄ (bytÄ), ba dokonce v jednĂ© mĂstnosti v prĆŻbÄhu dne. Bez tÄchto zĂĄznamĆŻ tedy nebudeme schopni relevantnÄ porovnĂĄvat vĂœslednĂ© hodnoty. MÄĆenĂ a hodnocenĂ bude realizovĂĄno ve dvou samostatnĂœch kategoriĂch, pro plĂsnÄ a bakterie.
2 Metody sbÄru dat o mikrobiĂĄlnĂm zneÄiĆĄtÄnĂ
Z hlediska expozice ÄlovÄka je zĂĄsadnĂ vĂœskyt mikroorganismĆŻ ve vdechovanĂ©m vzduchu. Tato hodnota je ovĆĄem s poÄasĂm, provozem budovy, vÄtrĂĄnĂm a promÄnlivĂœmi vnitĆnĂmi zdroji znaÄnÄ kolĂsavĂĄ. Proto se takĂ© sleduje vĂœskyt mikroorganismĆŻ na povrĆĄĂch nebo v prachu, kterĂœ je vÄtĆĄinou jejich zĂĄsobĂĄrnou. PomÄrnÄ rozsĂĄhlĂœ popis moĆŸnostĂ sbÄrĆŻ vzorkĆŻ je podrobnÄji rozebrĂĄn v [3]. Jsou zde takĂ© porovnĂĄny vĂœsledky rĆŻznĂœch mÄĆenĂ a je upozornÄno na skuteÄnost, ĆŸe samotnĂĄ technika sbÄru a pouĆŸitĂ© pĆĂstroje majĂ vliv na vĂœsledek, tudĂĆŸ lze vĂœsledky rĆŻznĂœch pracovnĂch skupin obtĂĆŸnÄ srovnĂĄvat. TradiÄnĂ metody spoÄĂvajĂ ve zjiĆĄtÄnĂ poÄtu ĆŸivotaschopnĂœch jednotek, tedy tÄch, kterĂ© jsou schopny se za pĆĂznivĂœch podmĂnek rozmnoĆŸovat. Metody se dÄlĂ na:
- aktivnĂ, kdy se vzduch nasĂĄvĂĄ nucenÄ tak, aby ÄĂĄsteÄky ulpÄly na ĆŸivnĂ© pĆŻdÄ a
- pasivnĂ, kterĂ© vyuĆŸĂvajĂ volnĂ©ho pohybu spor plĂsnĂ a bakteriĂ ve vzduchu a jejich samovolnĂ©ho usazovĂĄnĂ na ĆŸivnou pĆŻdu, pĆĂpadnÄ na rĆŻznĂ© povrchy, ze kterĂœch lze usazenĂœ bioaerosol odebrat.
NĂĄslednÄ se mikroorganismĆŻm vytvoĆĂ vhodnĂ© prostĆedĂ pro rĆŻst (jsou stanoveny teploty a kultivaÄnĂ doba). Po kultivaci se vyhodnotĂ kvantitativnÄ poÄet koloniĂ, pĆĂp. druhovĂĄ skladba. Aby byly vytvoĆeny vhodnĂ© podmĂnky pro obÄ sledovanĂ© skupiny, jsou ĆŸivnĂ© pĆŻdy odliĆĄnĂ© pro plĂsnÄ (vlĂĄknitĂ© mikromycety) popĆ. kvasinky a bakterie.
2.1 StanovenĂ mnoĆŸstvĂ mikroorganismĆŻ ve vzduchu [KTJ/m3]
VyhlĂĄĆĄka [1] uvĂĄdĂ, ĆŸe odbÄr vzorku vzduchu se provĂĄdĂ aeroskopem podle standartnĂho operaÄnĂho postupu uvedenĂ©ho v pĆĂloze a kultivacĂ na ĆŸivnĂ© pĆŻdÄ. PĆedpis popisuje pĆĂpravu prostor, jejich nutnost vyvÄtrĂĄnĂ a omezenĂ provozu, a to jak nucenÄ, tak pĆirozenÄ vÄtranĂœch, a nĂĄslednÄ postup a umĂstÄnĂ aeroskopu pĆi vlastnĂm odbÄru. Metoda aktivnĂho nasĂĄvĂĄnĂ vzduchu aeroskopem je zatĂm jedinĂĄ varianta, kterĂĄ je dle uzĂĄkonÄnĂœch pĆedpisĆŻ porovnatelnĂĄ s limitnĂ hodnotou, kdy za vyhovujĂcĂ se povaĆŸuje, nepĆekroÄili vzorek limit 500 KTJ/m3.
Aeroskop je zaĆĂzenĂ, kterĂ© pomocĂ zabudovanĂ©ho ventilĂĄtoru nucenÄ nasĂĄvĂĄ vzduch ve zkoumanĂ©m prostĆedĂ, a ÄĂĄstice obsaĆŸenĂ© v nasĂĄvanĂ©m vzduchu jsou zachyceny na ĆŸivnĂ© pĆŻdÄ. Princip odstĆedivĂ©ho aeroskopu je na obr. 2.
![Obr. 2a – OdstĆedivĂœ aeroskop, nasĂĄvanĂ© ÄĂĄstice jsou odstĆedivou silou unĂĄĆĄeny k agarovĂ©mu stripu (pĂĄsku) po obvodÄ hlavy [4]](/docu/clanky/0129/012972o2.jpg)
Obr. 2a – OdstĆedivĂœ aeroskop, nasĂĄvanĂ© ÄĂĄstice jsou odstĆedivou silou unĂĄĆĄeny k agarovĂ©mu stripu (pĂĄsku) po obvodÄ hlavy [4]
![Obr. 2b – Aeroskop pĆipravenĂœ k pouĆŸitĂ [4]](/docu/clanky/0129/012972o3.jpg)
Obr. 2b – Aeroskop pĆipravenĂœ k pouĆŸitĂ [4]
Toto mÄĆenĂ jsme provĂĄdÄli, protoĆŸe se jednĂĄ o stÄĆŸejnĂ parametr stavu vzduchu v mĂstnosti pro hlavnĂ obytnou mĂstnost v rodinnĂ©m domÄ, bÄĆŸnÄ obĂœvacĂ pokoj s kuchyĆskĂœm koutem, a pro jednu mĂ©nÄ zatĂĆŸenou mĂstnost, nejÄastÄji dÄtskĂœ pokoj. K tomu jsme samozĆejmÄ pro Ășplnost provedli odbÄr takĂ© ve venkovnĂm prostĆedĂ, vĆŸdy samostatnÄ pro celkovĂ© poÄty mikroorganismĆŻ (zejmĂ©na bakteriĂ) CPM a pro plĂsnÄ. Rozhodli jsme se pro mÄĆenĂ v uzavĆenĂ© mĂstnosti v dĂœchacĂ zĂłnÄ bez toho, aby mĂstnost byla pĆedem vyvÄtrĂĄna, neboĆ„ chceme postihnout situaci takovou, jakĂĄ reĂĄlnÄ v domÄ je. V pĆĂpadÄ, ĆŸe mĂstnost disponuje nucenĂœm vÄtrĂĄnĂm, bylo vĆŸdy zapnuto, aby bylo moĆŸnĂ© vliv provozu vzduchotechniky postihnout.
2.2 StanovenĂ poÄtu mikroorganismĆŻ na povrĆĄĂch [KTJ/m2]

 Obr. Ä. 3. – OdbÄr stÄru na definovanĂ© ploĆĄe stÄny s pomocĂ ĆĄablony a z talĂĆovĂ©ho ventilu
Obr. Ä. 3. – OdbÄr stÄru na definovanĂ© ploĆĄe stÄny s pomocĂ ĆĄablony a z talĂĆovĂ©ho ventiluToto mÄĆenĂ umoĆŸnĂ identifikovat zejmĂ©na zatĂĆŸenĂ stÄn nebo kritickĂœch stavebnĂch detailĆŻ plĂsnÄmi, coĆŸ je uĆŸiteÄnĂ© ve spornĂœch pĆĂpadech, kdy nĂĄrĆŻst plĂsnĂ nenĂ viditelnĂœ, ale zvĂœĆĄenĂĄ vlhkost zdiva umoĆŸĆuje vhodnĂ© podmĂnky pro osĂdlenĂ. OdbÄr vzorku je moĆŸnĂœ otiskem nebo stÄrem vlhkou houbiÄkou Äi tamponem z urÄitĂ© plochy. My jsme se zamÄĆili na monitoring stavu prvkĆŻ vzduchotechniky, kterĂĄ uĆŸ i v rodinnĂœch domech nenĂ zcela ojedinÄlĂĄ. Sledovali jsme vĂœskyt mikrobĆŻ na vnitĆnĂch povrĆĄĂch vzduchotechnickĂ© jednotky a na koncovĂœch elementech rozvodĆŻ vzduchu v interiĂ©ru. Aby bylo moĆŸnĂ© odebĂrat vzorek i tvarovÄ sloĆŸitÄjĆĄĂ plochy, pouĆŸĂvali jsme mÄkkĂ© houbiÄky. VlastnĂ houbiÄka je napuĆĄtÄna roztokem podporujĂcĂ ĆŸivotaschopnost mikroorganismĆŻ a je sterilnÄ zabalena.
Velmi podstatnĂœm Ășdajem je stanovenĂ velikosti odbÄrovĂ© plochy. Ta musĂ bĂœt dodrĆŸena u vĆĄech jednotlivĂœch stÄrĆŻ. Jako vhodnĂ© se jevĂ vytvoĆit si ĆĄablony (rĂĄmeÄky), pĆĂpadnÄ rĆŻznĂ© tvary ĆĄablon, kterĂ© majĂ tuto plochu pevnÄ danou a nemĆŻĆŸe tak dojĂt k nepĆesnostem v jednotlivĂœch odbÄrech. DĂĄle se jako vhodnĂ© jevĂ odebrat tyto stÄry na vĂce mĂstech a pĆedevĆĄĂm na tÄch, kterĂĄ jsou podezĆelĂĄ z pĆĂtomnosti plĂsnĂ, Äi bakteriĂ (viditelnĂœ rĆŻst mikroorganismĆŻ, chladnĂ© a vlhkĂ© plochy). VlastnĂ odbÄr vzorku „stÄr“ je tĆeba provĂĄdÄt tak, aby houbiÄka nebyla kontaminovĂĄna jinĂœmi ÄĂĄsticemi, neĆŸ jsou pĆedem stanovenĂ© plochy. UkĂĄzka odbÄru vzorkĆŻ je na obrĂĄzcĂch 3 a 4. VhodnĂ© je pouĆŸĂvat sterilnĂ rukavice a dbĂĄt na rychlĂ© provedenĂ odbÄru vzorku. Po provedenĂ stÄru z definovanĂ© plochy je zapotĆebĂ odebranĂœ vzorek (houbiÄku, tampon) opÄt neprodyĆĄnÄ uzavĆĂt tak, aby nedoĆĄlo k dalĆĄĂ expozici jinĂœmi mikroorganismy. NasbĂranĂ© vzorky je tĆeba uchovat v chladu a co nejdĆĂve je zpracovat.
2.3 PasivnĂ spadovĂĄ metoda [KTJ/Petriho miska.Äas]
Tato nejstarĆĄĂ metoda pouĆŸĂvanĂĄ jiĆŸ v 19. stoletĂ je zaloĆŸenĂĄ na prostĂ© sedimentaci bioaerosolu na ĆŸivnou pĆŻdu, na kterĂ© je nĂĄslednÄ kultivovĂĄn. JednĂĄ se o metodu velmi citlivou na proudÄnĂ vzduchu v mĂstnosti. Proto je tĆeba pĆed zapoÄetĂm odbÄru vzorku zajistit, aby v mĂstnosti nedochĂĄzelo k prĆŻvanu, Äi pohybu osob a pĆĂpadnÄ zabrĂĄnit dalĆĄĂmu vĂĆenĂ vzduchu ve sledovanĂ©m prostoru. ĆœivnĂĄ pĆŻda je nanesena na Petriho misce, coĆŸ jsou mÄlkĂ© sklenÄnĂ© nebo plastovĂ© misky s volnÄ pĆilĂ©hajĂcĂm vĂÄkem uĆŸĂvanĂ© v mikrobiologii jiĆŸ od 2. poloviny 19. stoletĂ, pojmenovanĂ© po nÄmeckĂ©m bakteriologovi J. R. Petrim (asistentovi R. Kocha). MĂĄ prĆŻmÄr 9 cm a doba sbÄru se doporuÄuje mezi 10 a 30 minutami. Je natolik v mikrobiologickĂ© praxi zabÄhlĂĄ, ĆŸe se pouĆŸĂvĂĄ i jako mĂra plochy bez pĆepoÄĂtĂĄvĂĄnĂ na bÄĆŸnĂ© jednotky SI. HmotnĂ© ÄĂĄstice volnÄ sedimentujĂ na ĆŸivnou pĆŻdu a jejich zachycenĂ© mnoĆŸstvĂ je samozĆejmÄ na Äase zĂĄvislĂ©, pro ĂșÄely hodnocenĂ prostĆedĂ v budovĂĄch se nejÄastÄji uĆŸĂvĂĄ doby 4 h.
Po odbÄru jsou misky opÄt uzavĆeny, aby nedoĆĄlo k neĆŸĂĄdoucĂ kontaminaci. ĆœivnĂ© pĆŻdy v miskĂĄch zajiĆĄĆ„ujĂ optimĂĄlnĂ pĆĂsun ĆŸivin pĆi kultivaci mikroorganismĆŻ. ĆœivnĂœch pĆŻd je celĂĄ Ćada, liĆĄĂ se sloĆŸenĂm, ĂșÄelem pouĆŸitĂ a selektivitou. Je tĆeba vĆŸdy u vzorkĆŻ rozliĆĄovat Petriho misky, na kterĂœch budou vĆŸdy kultivovĂĄny bakterie nebo plĂsnÄ. Tyto misky zpravidla obsahujĂ odliĆĄnĂ© ĆŸivnĂ© pĆŻdy, kterĂ© mohou inhibovat ostatnĂ skupiny mikroorganismĆŻ. Sedimentaci na Petriho miskĂĄch jsme pouĆŸili jako doplĆkovĂ© mÄĆenĂ stavu vnitĆnĂho vzduchu, v hlavnĂ pobytovĂ© a jednĂ© klidnÄjĆĄĂ mĂstnosti domu a takĂ© ve venkovnĂm prostoru. Budeme rovnÄĆŸ v dalĆĄĂm sledovat, zda vĂœsledky aktivnĂ a pasivnĂ metodou vzorkovĂĄnĂ vzduchu spolu korelujĂ. OdbornĂĄ literatura uvĂĄdĂ, ĆŸe vzĂĄjemnĂĄ souvislost je neprĆŻkaznĂĄ, coĆŸ tĂmto dvojitĂœm mÄĆenĂm mĆŻĆŸeme ovÄĆit, Äi za specifickĂœch podmĂnek vyvrĂĄtit.
Petriho misky s pĆĂsluĆĄnou ĆŸivnou pĆŻdou jsou otevĆeny aĆŸ na mĂstÄ provĂĄdÄnĂ odbÄru, kde jsou vystaveny vĆŸdy po stejnĂœ ÄasovĂœ interval zkoumanĂ©mu prostĆedĂ a ponechĂĄny pĆirozenĂ©mu prĆŻbÄhu sedimentace pevnĂœch ÄĂĄstic. Doba expozice se musĂ uzpĆŻsobit oÄekĂĄvanĂ©mu mnoĆŸstvĂ mikroorganismĆŻ. U pĆĂliĆĄ krĂĄtkĂ©ho Äasu expozice bude poÄet ĆŸivotaschopnĂœch organismĆŻ vykultivovanĂœch na ĆŸivnĂ© pĆŻdÄ neprĆŻkaznÄ nĂzkĂœ a po dlouhĂ© dobÄ naopak zase natolik mohutnĂœ, ĆŸe nebude moĆŸnĂ© na miskĂĄch rozliĆĄit jednotlivĂ© kolonie. UkĂĄzka vykultivovanĂœch plĂsnĂ a bakteriĂ je prezentovĂĄna na obr. Ä. 5. Po uplynutĂ Äasu expozice je nutnĂ© Petriho misky opÄt uzavĆĂt a co nejdĆĂve umĂstit do optimĂĄlnĂch kultivaÄnĂch podmĂnek.
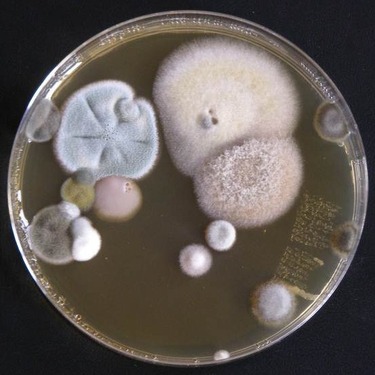
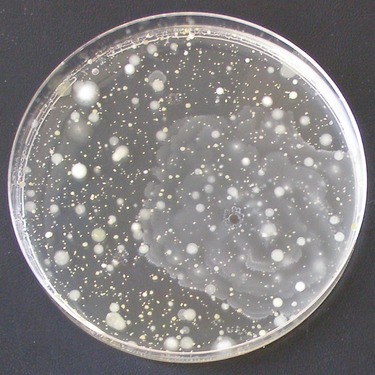 Obr. Ä. 5. – UkĂĄzka jiĆŸ kultivovanĂœch vzorkĆŻ na Petriho miskĂĄch; vlevo: plĂsnÄ; vpravo: bakterie
Obr. Ä. 5. – UkĂĄzka jiĆŸ kultivovanĂœch vzorkĆŻ na Petriho miskĂĄch; vlevo: plĂsnÄ; vpravo: bakterie2.4 StanovenĂ koncentrace v prachu [KTJ/g]
Toto vyĆĄetĆenĂ je uĆŸiteÄnĂ© v pĆĂpadech, kdy se v prostĆedĂ vyskytuje vÄtĆĄĂ mnoĆŸstvĂ prachu, kterĂœ lze odebrat. Jeho sloĆŸenĂ je totiĆŸ podstatnÄ stabilnÄjĆĄĂ neĆŸ aktuĂĄlnĂ stav vzduchu a literatura uvĂĄdĂ, ĆŸe je tĂ©ĆŸ Äasto vĂœbornou ĆŸivnou pĆŻdou pro mikroorganismy, zejmĂ©na prach v domĂĄcnostech, kterĂœ obsahuje organickĂ© neÄistoty, ĆĄupinky lidskĂ© kĆŻĆŸe apod. V 1 g domĂĄcĂho prachu se mohou nachĂĄzet tisĂce ĆŸivotaschopnĂœch (kultivovatelnĂœch) mikroorganismĆŻ. Toto vyĆĄetĆenĂ jsme provĂĄdÄli jen jako doplĆkovĂ©, pro snĂmĂĄnĂ mĂĄlo praĆĄnĂœch povrchĆŻ jsme vyuĆŸĂvali kontaktnĂ otisky.
3 Kultivace a vyhodnocenĂ vzorkĆŻ
CelĂœ proces kultivace plĂsnĂ a bakteriĂ je popsĂĄn v ÄSN [6] a [7] a na tyto normy se odkazuje takĂ© VyhlĂĄĆĄka Ä. 6 ze dne 16. prosince 2002 [1]. Kultivace ĆŸivĂœch organismĆŻ zachycenĂœch pĆĂmo na ĆŸivnĂœch pĆŻdĂĄch (aeroskop, spad, otisky) probĂhĂĄ pĆĂmo na tĂ©to pĆŻdÄ. Pokud je vzorek odebrĂĄn na pomocnĂœ materiĂĄl, jakĂœm je napĆ. houbiÄka pro stÄry, nebo je odebrĂĄn vzorek prachu, je tĆeba vzorek vhodnou metodou uvolnit, naĆedit a nĂĄslednÄ na ĆŸivnou pĆŻdu pĆenĂ©st. TÄchto technik je vĂce, coĆŸ je opÄt dĆŻvodem, proÄ vĂœsledky zĂskanĂ© rĆŻznĂœmi metodami nebo stejnĂœmi metodami s odliĆĄnĂœm zpracovĂĄnĂm nelze vzĂĄjemnÄ porovnĂĄvat. Proto je nutnĂ© pĆistupovat pĆi hodnocenĂ opatrnÄ s porovnĂĄvĂĄnĂm vĂœsledkĆŻ dosaĆŸenĂœch jinĂœmi autory. PĆi sbÄru i zpracovĂĄnĂ vzorkĆŻ jsme tedy dbali na to, aby sbÄr provĂĄdÄli stejnĂ pracovnĂci, stejnou technikou, a zpracovĂĄnĂ vzorkĆŻ bylo provedeno jednou laboratoĆĂ. TĂm jsme dosĂĄhli sice malĂ©ho, za to vĆĄak konzistentnĂho souboru dat k hodnocenĂ. Kultivaci vzorkĆŻ a odbornĂœ dohled nad jejich zpracovĂĄnĂm provĂĄdÄli zamÄstnanci pracoviĆĄtÄ Mikrobiologie Ăstavu agrochemie, pĆŻdoznalstvĂ, mikrobiologie a vĂœĆŸivy rostlin Mendelovy univerzity v BrnÄ. AeroskopickĂ© mÄĆenĂ provĂĄdÄli pracovnĂci ZdravotnĂho Ășstavu.
Kultivace bakteriĂ
ZpracovanĂ© vzorky urÄenĂ© pro kultivaci se umĂstĂ do biologickĂ©ho termostatu s teplotou nastavenou na 30 °C ±1 °C na dobu 72 hodin. Tam za danĂœch podmĂnek pĆi aerobnĂ inkubaci vyrostou na pĆĂsluĆĄnĂ© ĆŸivnĂ© pĆŻdÄ kolonie bakteriĂ, kterĂ© se nĂĄslednÄ spoÄĂtajĂ.
Kultivace plĂsnĂ
ZpracovanĂ© vzorky se obdobnÄ umĂstĂ do biologickĂ©ho termostatu, ovĆĄem jiĆŸ s jinou teplotou, kterĂĄ je nastavena na 25 °C ±1 °C na 3–5 dnĆŻ. Po uplynutĂ inkubace se vzorky vyjmou a spoÄĂtajĂ poÄty koloniĂ tvoĆĂcĂch jednotky.
VyhodnocenĂ
VlastnĂ vyhodnocenĂ jiĆŸ kultivovanĂœch vzorkĆŻ se provĂĄdĂ napĆ. pomocĂ ÄĂtaÄĆŻ koloniĂ, viz obr. 6.
4 ZĂĄvÄr
ÄlĂĄnek popisuje postup, jakĂœm je moĆŸnĂ© vytvoĆit soubor vzorkĆŻ a nĂĄslednÄ dat, ze kterĂœch je moĆŸnĂ© zĂskat obraz o stavu sledovanĂœch prostor. Je zde snaha poukĂĄzat na nutnost pĆedem stanovit pevnĂĄ pravidla, jako ÄasovĂ© intervaly expozice Petriho misek, mĂsta a poÄet odbÄrĆŻ a dalĆĄĂ okrajovĂ© podmĂnky, bez kterĂœch jinak nenĂ moĆŸnĂ© vzorky zĂskanĂ© z rĆŻznĂœch budov porovnĂĄvat. OdbornĂĄ literatura, kterĂĄ se touto problematikou zabĂœvĂĄ, je dominantnÄ zahraniÄnĂ a jejĂ autoĆi jsou mikrobiologovĂ©. Najdeme zde pomÄrnÄ rozsĂĄhlĂ© soubory dat s odpovĂdajĂcĂm statistickĂœm zpracovĂĄnĂm, kvantifikaci a identifikaci zachycenĂœch mikroorganismĆŻ, ovĆĄem Ășdaje o prostĆedĂ, ze kterĂ©ho byly odebrĂĄny, jsou pomÄrnÄ kusĂ©. NejvĂœĆĄe se dozvĂme materiĂĄlovĂ© ĆeĆĄenĂ konstrukÄnĂho systĂ©mu, ale o zpĆŻsobu vÄtrĂĄnĂ, vytĂĄpÄnĂ a dalĆĄĂch technickĂœch aspektech velmi mĂĄlo. NaĆĄe ĆĄetĆenĂ pĆispĂvĂĄ k souÄasnĂ©mu vÄdÄnĂ tĂm, ĆŸe prĂĄvÄ tyto aspekty zdĆŻrazĆuje a hledĂĄ v nich souvislosti.
Literatura
- [1] Äesko; VyhlĂĄĆĄka Ä. 6 ze dne 16. prosince 2002, kterou se stanovĂ hygienickĂ© limity chemickĂœch, fyzikĂĄlnĂch a biologickĂœch ukazatelĆŻ pro vnitĆnĂ prostĆedĂ pobytovĂœch mĂstnostĂ nÄkterĂœch staveb. In: SbĂrka zĂĄkonĆŻ Ä. 6/2003, ÄĂĄstka 4. DostupnĂ© z: http://aplikace.mvcr.cz/sbirka-zakonu/
- [2] HAAS A., HABIB J., LUXNER J. a kol; Comparison of background levels of culturable fungal spore
- concentrations in indoor and outdoor air in southeastern Austria in Atmospheric Environment 98 (2014), str. 640-647
- [3] WANNER H. a kol.; EUR 14988 - Enviromnment Institut: Indoor air quality & int impact on man, No. 12 Biological Particles in Indoor Environments; Commission of the european communites; 1993 Luxembourg, Zdroj:
http://vetrani.tzb-info.cz/vnitrni-prostredi/12819-mikrobialni-mikroklima-budov-i - [4] Labpak; AirSampler,. Dostupné z https://www.prlabs.co.uk/news/downloads/K9FweVWR%20Surface%20Air
- [5] ÄSN ISO 7954. Mikrobiologie. VĆĄeobecnĂ© pokyny pro stanovenĂ poÄtu kvasinek a plĂsnĂ. Technika poÄĂtĂĄnĂ koloniĂ vykultivovanĂœch pĆi 25 °C.
- [6] ÄSN EN ISO 4833. Mikrobiologie. VĆĄeobecnĂ© pokyny pro stanovenĂ celkovĂ©ho poÄtu mikroorganismĆŻ. Technika poÄĂtĂĄnĂ koloniĂ vykultivovanĂœch pĆi 30 °C.
PĆĂspÄvek vznikl za podpory specifickĂ©ho vĂœzkumu VUT FAST-S-15-2620 a vÄdeckĂ©ho centra Admas.
PosuzovanĂĄ prĂĄce se vÄnuje aktuĂĄlnĂmu problĂ©mu mikrobiĂĄlnĂ kontaminace obytnĂœch prostor a metodĂĄm jak mĂru tĂ©to kontaminace zjiĆĄĆ„ovat. Jsou zde popisovĂĄny standardnĂ metody analĂœzy mikrobiĂĄlnĂ kontaminace vzduchu a dĂĄle metody stanovenĂ kontaminace rĆŻznĂœch povrchĆŻ. AutoĆi se snaĆŸĂ struÄnou a srozumitelnou formou seznĂĄmit ne ĂșplnÄ zasvÄcenĂ©ho ÄtenĂĄĆe s touto do jistĂ© mĂry sloĆŸitou problematikou.
This part focuses on the issue of collecting samples of the microbial environment in the houses near Brno. The aim is to find suitable methods that are applicable in practice, reasonably expensive and describe well the state of the microbial element of environment, in order not only to evaluate air quality, but also to find the source of detected state. Investigations were carried out in houses equipped with air condition and also compared with natural ventilation.

