Průběh dlouhodobého testu denitrifikace
Denitrifikační bioreaktory slouží k odstranění dusičnanů ze smyvů v zemědělských oblastech, které by se jinak prostřednictvím povrchového odtoku z těchto polí dostaly do vodních toků. Průběh denitrifikačního procesu a jeho rychlost je ovlivněna řadou faktorů. Významným faktorem je kvalita vody přitékající do denitrifikačního bioreaktoru, která je znečištěna kromě dusičnanů i jinými polutanty, jako jsou pesticidy. Byla navržena a optimalizována metodika dlouhodobého testování vlivu pesticidních látek na průběh denitrifikace. Navržený jednorázový test umožňuje vyhodnotit inhibici denitrifikační rychlosti. Byla provedena optimalizace dávky dusičnanů (15 mg/l), způsob dávkování a nejpříznivější koncentrace NaHCO3 (0,5 g/l) v deionizované vodě.

Článek byl vydán v rámci odborné konference doktorského studia Juniorstav 2021. Byl oceněn odbornou porotou konference a okomentován spolupracovníky redakce TZB Info.
1. Úvod
V dnešní době způsobují některé činnosti spojené s hnojením dusíkem v zemědělských oblastech zvýšené koncentrace dusičnanů v povrchových a podzemních vodách [1]. Dusičnany patří mezi migrační formu dusíku, která se snadno hromadí v přírodních vodách, což vede ke zhoršení kvality vody [2], [3]. Výsledkem je eutrofizace, rozkvět toxických řas, ztráta biodiverzity a kontaminace pitné vody. K odstraňování NO3 z vody jsou široce používány bioreaktory na bázi dřevní štěpky [1].
Denitrifikační bioreaktory jsou relativně jednoduchou pasivní technologií [4], jedná se o účinnou metodu pro odstraňování dusičnanů z podzemních vod a odtoků ze zemědělsky obhospodařovaných ploch. Denitrifikační bioreaktory jsou v podstatě kontejnery naplněné různými typy pevných organických látek, nejčastěji dřevní štěpkou [5]. Tato metoda je založena na anaerobní redukci dusičnanů heterotrofními bakteriemi a používá pevný zdroj organického uhlíku pro růst denitrifikačních bakterií [6]. Dřevní štěpka je nejběžněji a nejúspěšněji používaným zdrojem uhlíku v mnoha studiích, kvůli její vysoké hodnotě propustnosti, nízkým nákladům na materiál, vysokému poměru C/N a dlouhodobé odolnosti [1]. Průběh denitrifikace s náplní z dřevní štěpky je významně ovlivněn typem zdroje uhlíku, teplotou, pH a rozpuštěným kyslíkem [7], [8].
Ze zemědělsky obhospodařovaných ploch odtéká voda, která je kontaminována nejen dusičnany, ale také dalšími polutanty. Dle Schulze [9] se odhaduje, že 10 % pesticidů, které byly aplikované na půdu, zasahují necílové oblasti, zejména však oblasti podél polí. Odhadované hodnoty ztrát jsou však podmíněné počasím [10]. Přítomnost pesticidů v ekosystémech má nepříznivé účinky, které se liší v závislosti na koncentraci kontaminantu, množství a době expozice [11], [12]. Je proto logické položit jsi otázku, zda tyto látky nenarušují denitrifikační proces a do jaké míry jsou technologií denitrifikačních bioreaktorů odstraňovány z kontaminované vody. Denitrifikace může podporovat biodegradaci pesticidů. To bylo prokázáno u atrazinu [13] a chloracetanilidových pesticidů [14].
Cílem výzkumu je proto navrhnout metodiku pro studium osudu vybraných pesticidů v průběhu denitrifikace, zejména jejich biotransformace a adsorpce na náplň reaktoru a vliv na denitrifikační proces. Studie se zabývá návrhem dlouhodobého testu a optimalizací jednotlivých parametrů, jako jsou počáteční koncentrace N-NOX, množství a způsob dávkování roztoku KNO3 pro udržení příznivé koncentrace dusičnanů a také potřebnou dávkou NaHCO3.
2. Metodika
Princip a provedení testu
Jednorázový laboratorní test byl simulován ve 2litrové lahvi, která slouží jako modelový denitrifikační bioreaktor. Bylo použito 12 lahví, kde každá láhev obsahovala 25 g topolových hoblin, frakce 1,0–1,5 cm a 2000 ml deionizované vody obohacené o KNO3 a NaHCO3. Pro vytvoření anoxického prostředí se lahev probublala argonem, až koncentrace O2 klesla pod 0,5 mg/l. Lahve se následně uzavřely a inkubovaly v termostatu při T = 20 °C bez přístupu světla.
Pokus byl ukončen v dílčích inkubačních dobách vždy ve třech lahvích po 7, 14, 21 a 28 dnech, všechny vzorky byly po ukončení zpracovány pomocí následujících postupů. Byly změřeny hodnoty pH, O2, CHSKCr, PC, N-NH4, N-NO2 a koncentrace N-NOX. Po změření koncentrace N-NOX v každé ze tří lahví byl výpočtem stanoven průměr. Na základě stanoveného průměru koncentrace N-NOX, byla vypočtena dávka roztoku KNO3 (10 000 mg/l), tak aby byla koncentrace dusičnanů identická s počáteční hodnotou. Určená dávka roztoku KNO3 byla nadávkována do zbývajících lahví, které se poté uložily do termostatu.
Průběh denitrifikace je hodnocen na základě inhibice denitrifikační rychlosti, která je vypočtena jako množství odstraněného dusičnanového dusíku za časovou jednotku.
Pro stanovení vybraných ukazatelů byly použity následující analytické metody. Hodnoty pH a O2, byly měřeny pomocí multimetru Hach HQ40D (Loveland, Colorado, USA). CHSKCr byla stanovena semi-mikrometodou s dichromanem draselným v kyselém prostředí a výpočet byl proveden na základě rozdílu intenzity zbarvení při 445 nm. Celkový fosfor PC byl měřen spektrofotometricky s molybdenovou modří, při vlnové délce 690 nm. Analýza N-NH4 byla změřena spektrofotometricky pomocí Nesslerova činidla, při vlnové délce 425 nm. N-NO2 byly stanoveny spektrofotometricky s α-naftolem, na základě rozdílu intenzity zbarvení při 515 nm. Stanovení N-NOX bylo provedeno pomocí absorpční UV metody na optické sondě Nitratax plus sc Sensor (Loveland, Colorado, USA).
Vstupní koncentrace N-NOX
S ohledem na přírodní podmínky a předchozí provedené pokusy [15] byly zkoušené vstupní koncentrace N-NOX 15 mg/l a 30 mg/l. Tyto počáteční koncentrace jsou vhodné pro udržení denitrifikačních podmínek pokusu po dílčí inkubační dobu sedmi dnů. Zvolené koncentrace byly odzkoušeny paralelně podle navržené metodiky.
Dávka NaHCO3, pH
Byl zkoumán vliv dávky hydrogenuhličitanu sodného na rychlost denitrifikace. Vstupní parametry testu byly 25 g topolových hoblin, frakce 1,0–1,5 cm, koncentrace N-NOX 15 mg/l. Zkoušené dávky NaHCO3: 0 g/l, 0,5 g/l, 1 g/l a 2 g/l. Každá dávka byla ve třech opakováních a po dílčích inkubačních dobách byly ve všech lahvích změřeny vybrané parametry a pokus se neukončoval. Pipetou bylo odebráno z každé lahve 25 ml vzorku pro stanovení N-NOX. Dále byly změřeny vybrané parametry, a to pH, koncentrace O2 a CHSKCr. Do každé lahve bylo nadávkováno potřebné množství roztoku KNO3 stanovené výpočtem, tak aby byla koncentrace N-NOX 15 mg/l. Po stanovení a nadávkování roztoku KNO3 byly lahve znovu uzavřeny a inkubovány v termostatu při T = 20 °C bez přístupu světla.
3. Výsledky a diskuse
Vstupní koncentrace N-NOX
Na Obr. 1 je znázorněno srovnání dvou testovaných koncentrací N-NOX, 15 mg/l a 30 mg/l. Při počáteční koncentraci 30 mg/l probíhala denitrifikace kontinuálně do konce první inkubační doby (sedm dní). Po nadávkování roztoku KNO3 vzrostla hodnota koncentrace N-NOX na 30 mg/l. Při měření po dalších inkubačních dobách byly hodnoty koncentrace N-NOX nad hodnotu 30 mg/l. Průměrná denitrifikační rychlost se snížila z hodnoty 3,46 mg/l/d na 0 mg/l/d, proces denitrifikace se zastavil.
Při testovaní koncentrace 15 mg/l N-NOX, probíhal denitrifikační proces s minimálními změnami denitrifikační rychlosti i po nadávkování roztoku KNO3 každý týden. V průběhu měření se průměrná rychlost denitrifikace po dílčích inkubačních dobách zvyšovala, z 1,65 mg/l/d na hodnotu 1,84 mg/l/d. V posledním týdnu pokusu byla naopak nejnižší 1,00 mg/l/d.
Koncentrace kyslíku na konci testů byla u koncentrace N-NOX 15 mg/l 0,54 ± 0,06 mg/l a u 30 mg/l mírně vyšší 0,58 ± 0,12 mg/l. CHSKCr v průběhu testů se výrazně neodlišovala, naměřené hodnoty byly v rozmezí od 90 do 370 mg/l.
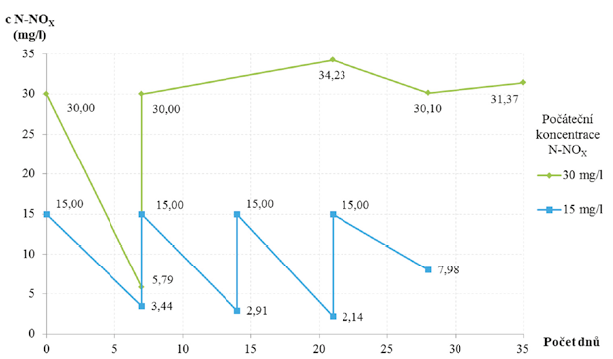
Obr. 1 Srovnání průběhů denitrifikace s počáteční koncentrací N-NOX 15 mg/l a 30 mg/l
Při počáteční koncentraci N-NOX 15 mg/l byl průběh denitrifikačního testu kontinuální a nedošlo k poklesu koncentrace N-NOX pod kritickou hodnotu. Při opakovaných testech s počáteční koncentrací 15 mg/l byly průběhy testů i průměrná rychlost denitrifikace srovnatelné, jak je patrné z Obr. 2. Průměrná denitrifikační rychlost byla nejvyšší u testu J, v rozmezí 1,0–1,84 mg/l/d. U testu L a M byly zaznamenány nižší hodnoty a to zejména v posledním týdnu testu, u testu L 0,45–1,55 mg/l/d a u testu M 0,66–1,80 mg/l/d. Po 21 dnech byl roztok KNO3 dávkován pouze u testu J, u zbývajících dvou byla koncentrace N-NOX dostatečná.
Odstraněný dusičnan může být přeměněn na dusitany, N2O a NH4+ [16]. Pan [17] a Li [18] tvrdí, že hodnota pH < 6,0 může způsobit nepříznivé účinky akumulace dusitanů nebo emise N2O. Podobné výsledky byly pozorovány i při dlouhodobém testu, při nižších hodnotách pH byly naměřené hodnoty koncentrace N-NO2 vyšší. Byly zaznamenány vyšší hodnoty N-NH4 u testu J. Dle Zhao [1], dřevní štěpka obecně uvolňuje vysoké N-NH4 během počáteční fáze, což vysvětluje zvýšené hodnoty u testu J. U dvou zbývajících testů byly hodnoty koncentrace N-NH4 stabilní, nejvyšší hodnota 0,63 mg/l.
Hodnoty CHSKCr na konci testů se pohybovaly od 73 do 240 mg/l. Toto množství CHSKCr je dostatečné pro podporu denitrifikace [19]. Koncentrace kyslíku v průběhu testu J nepřekročily výrazně hodnotu 0,5 mg/l. U testů L a M byla zaznamenána vysoká hodnota koncentrace kyslíku v každé dílčí inkubační době. Pro snížení koncentrace kyslíku byly lahve probublány argonem, tak, aby hodnota O2 byla < 0,5 mg/l. Nejvyšší hodnoty PC byly naměřeny u testu J 2,89–3,29 mg/l. U testu L byly hodnoty PC 1,16 ± 0,40 mg/l a u tesu M 1,17 ± 0,17 mg/l.
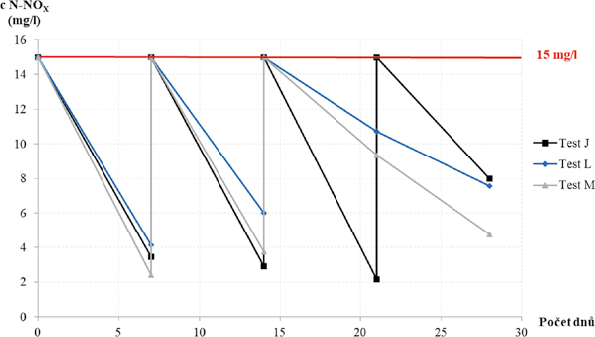
Obr. 2 Průběh denitrifikace s počáteční koncentrací N-NOX 15 mg/l
Dávka NaHCO3, pH
Na Obr. 3 jsou znázorněny průběhy hodnot pH při různých dávkách NaHCO3. U nejnižší dávky NaHCO3 0 g/l bylo pH v rozmezí od 7,04 až 8,55, naopak nejvyšší pH 8,15–9,17 u dávky 2 g/l. Dle Paule [20] je pH mezi 7,5 a 8,0 pro proces denitrifikace nejvhodnější. Optimum bylo u každé dávky překročeno na počátku testu, po vyluhování látek kyselého charakteru z hoblin po sedmi dnech kleslo pH pod hodnotu 8,0 pouze u dávky 0 g/l. Po 14 dnech se dostaly hodnoty do optimálního rozmezí u všech zkoušených dávek kromě dávky 2 g/l.
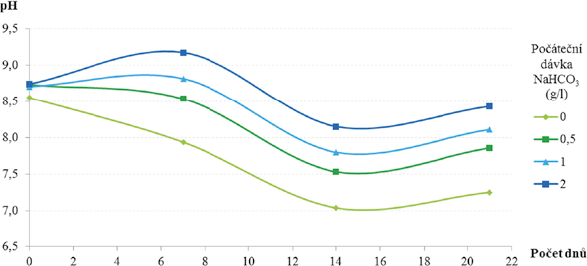
Obr. 3 Hodnoty pH v průběhu denitrifikace při různých dávkách NaHCO3
Obr. 4 znázorňuje průměrné denitrifikační rychlosti v průběhu testu s různými dávkami NaHCO3. Po první dílčí inkubační době byla nejvyšší průměrná denitrifikační rychlost u dávky 0 g/l, na konci testu však dosáhla nejvyšší pokles. Dávky 0,5 g/l a 1 g/l byly porovnatelné v průběhu celého testu. Nejvyšší průměrné denitrifikační rychlosti za celé sledované období byly zaznamenány při nejvyšší dávce NaHCO3 , a to 2 g/l. Tyto výsledky jsou v rozporu s Cao [21], který v studii zaznamenal, že rychlost denitrifikace rostla s klesajícím pH v rozmezí 6,5–9,2.
Hodnoty kyslíku během testu stoupaly nad 0,5 mg/l u všech zkoušených dávek, bylo nutné probublávání argonem. V průběhu testu byly hodnoty CHSKCr porovnatelné u všech dávek, v rozmezí od 79 do 170 mg/l, což je dostatečné pro podporu denitrifikace.
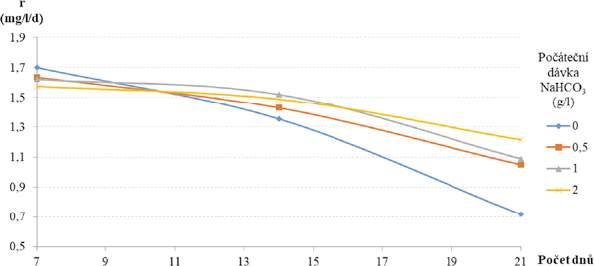
Obr. 4 Porovnání průměrné rychlosti v průběhu denitrifikace, při různých dávkách NaHCO3
4. Závěr
Při počáteční koncentraci N-NOX 15 mg/l, dávce NaHCO3 0,5 g/l, a dílčí inkubační době sedmi dnů byly dosaženy optimální denitrifikační podmínky pro 28denní test denitrifikace.
Metodika dlouhodobého testu je používána pro sledování chování vybraných pesticidních látek při denitrifikačních podmínkách.
Poděkování
Výzkum byl finančně podpořen v rámci Projektu specifického výzkumu FAST-J-20-6395, Degradace pesticidů v denitrifikačních bioreaktorech.
Použité zdroje
- ZHAO, Jiamin, Qiaochong HE, Nan CHEN, Tong PENG a Chuanping FENG. Denitrification behavior in a woodchip-packed bioreactor with gradient filling for nitrate-contaminated water treatment. Biochemical Engineering Journal [online]. 2020, 154 [cit. 2020-10-19]. ISSN 1369703X. Dostupné z:
https://www.sciencedirect.com/science/article/abs/pii/S1369703X19303936 - CANFIELD, Donald E., Alexander N. GLAZER a Paul G. FALKOWSKI. The Evolution and Future of Earth’s Nitrogen Cycle. Science [online]. 2010, 330(6001), 192-196 [cit. 2020-10-19]. ISSN 0036-8075. Dostupné z:
https://science.sciencemag.org/content/330/6001/192 - ZHANG, Yan, Fadong LI, Qiuying ZHANG, Jing LI a Qiang LIU. Tracing nitrate pollution sources and transformation in surface- and ground-waters using environmental isotopes. Science of The Total Environment [online]. 2014, 490, 213-222 [cit. 2020-10-19]. ISSN 00489697. Dostupné z:
https://www.sciencedirect.com/science/article/abs/pii/S0048969714006615 - WEIGELHOFER, Gabriele a Thomas HEIN. Efficiency and detrimental side effects of denitrifying bioreactors for nitrate reduction in drainage water. Environmental Science and Pollution Research [online]. 2015, 22(17), 13534-13545 [cit. 2020-08-26]. ISSN 0944-1344. Dostupné z: https://link.springer.com/article/10.1007/s11356-015-4634-0
- SCHIPPER, Louis A., Will D. ROBERTSON, Arthur J. GOLD, Dan B. JAYNES a Stewart C. CAMERON. Denitrifying bioreactors—An approach for reducing nitrate loads to receiving waters. Ecological Engineering [online]. 2010, 36(11), 1532-1543 [cit. 2019-11-10]. ISSN 09258574. Dostupné z:
https://www.sciencedirect.com/science/article/abs/pii/S0925857410000807 - ŠEREŠ, Michal, Klára Anna MOCOVÁ, Jabbar MORADI, Michal KRIŠKA, Vladimír KOČÍ a Tereza HNÁTKOVÁ. The impact of woodchip-gravel mixture on the efficiency and toxicity of denitrification bioreactors. Science of The Total Environment. 2019, 647, 888-894. ISSN 00489697. Dostupné z:
https://www.sciencedirect.com/science/article/abs/pii/S0048969718330110 - WARNEKE, Sören, Louis A. SCHIPPER, Michael G. MATIASEK, Kate M. SCOW, Stewart CAMERON, Denise A. BRUESEWITZ a Ian R. MCDONALD. Nitrate removal, communities of denitrifiers and adverse effects in different carbon substrates for use in denitrification beds. Water Research [online]. 2011, 45(17), 5463-5475 [cit. 2020-10-20]. ISSN 00431354. Dostupné z: https://www.sciencedirect.com/science/article/abs/pii/S004313541100443X
- ADDY, Kelly, Arthur J. GOLD, Laura E. CHRISTIANSON, Mark B. DAVID, Louis A. SCHIPPER a Nicole A. RATIGAN. Denitrifying Bioreactors for Nitrate Removal: A Meta-Analysis. Journal of Environmental Quality [online]. 2016, 45(3), 873-881 [cit. 2020-10-20]. ISSN 00472425. Dostupné z:
https://acsess.onlinelibrary.wiley.com/doi/full/10.2134/jeq2015.07.0399 - SCHULZ, Ralf. Field Studies on Exposure, Effects, and Risk Mitigation of Aquatic Nonpoint-Source Insecticide Pollution: A Review. Journal of Environmental Quality [online]. 2004, 33(2), 419-448 [cit. 2020-09-23]. ISSN 00472425. Dostupné z: https://acsess.onlinelibrary.wiley.com/doi/abs/10.2134/jeq2004.4190
- DE SOUZA, Renata Mariane, Daiana SEIBERT, Heloise Beatriz QUESADA, Fátima DE JESUS BASSETTI, Márcia Regina FAGUNDES-KLEN a Rosângela BERGAMASCO. Occurrence, impacts and general aspects of pesticides in surface water: A review. Process Safety and Environmental Protection [online]. 2020, 135, 22-37 [cit. 2020-10-19]. ISSN 09575820. Dostupné z: https://www.sciencedirect.com/science/article/abs/pii/S0957582019318683
- MARGNI, M., D. ROSSIER, P. CRETTAZ a O. JOLLIET. Life cycle impact assessment of pesticides on human health and ecosystems. Agriculture, Ecosystems & Environment [online]. 2002, 93(1-3), 379-392 [cit. 2020-08-26]. ISSN 01678809. Dostupné z: https://www.sciencedirect.com/science/article/abs/pii/S016788090100336X
- RICE, Pamela J., Patricia J. RICE, Ellen L. ARTHUR a Aldos C. BAREFOOT. Advances in Pesticide Environmental Fate and Exposure Assessments. Journal of Agricultural and Food Chemistry [online]. 2007, 55(14), 5367-5376 [cit. 2020-08-26]. ISSN 0021-8561. Dostupné z: https://pubs.acs.org/doi/10.1021/jf063764s
- DOUGLASS, James F., Mark RADOSEVICH a Olli H. TUOVINEN. Biomineralization of atrazine and analysis of 16S rRNA and catabolic genes of atrazine degraders in a former pesticide mixing site and a machinery washing area. Journal of Soils and Sediments [online]. 2016, 16(9), 2263-2274 [cit. 2020-10-19]. ISSN 1439-0108. Dostupné z:
https://link.springer.com/article/10.1007/s11368-016-1416-3 - CHEN, Zhongbing, Yi CHEN, Jan VYMAZAL, Lumír KULE a Milan KOŽELUH. Dynamics of chloroacetanilide herbicides in various types of mesocosm wetlands. Science of The Total Environment [online]. 2017, 577, 386-394 [cit. 2020-10-19]. ISSN 00489697. Dostupné z: https://www.sciencedirect.com/science/article/abs/pii/S0048969716324159
- PÁNIKOVÁ, Kristína. Vývoj testu inhibice denitrifikace. In: JUNIORSTAV 2020. Brno: ECON publishing, 2020, s. 515–521. ISBN 978-80-86433-73-8.
- HU, Rongting, Xilai ZHENG, Tianyuan ZHENG, Jia XIN, Huan WANG a Qiguo SUN. Effects of carbon availability in a woody carbon source on its nitrate removal behavior in solid-phase denitrification. Journal of Environmental Management [online]. 2019, 246, 832-839 [cit. 2020-10-19]. ISSN 03014797. Dostupné z:
https://www.sciencedirect.com/science/article/pii/S0301479719308588 - PAN, Yuting, Liu YE, Bing-Jie NI a Zhiguo YUAN. Effect of pH on N2O reduction and accumulation during denitrification by methanol utilizing denitrifiers. Water Research [online]. 2012, 46(15), 4832-4840 [cit. 2020-10-20]. ISSN 00431354. Dostupné z: https://www.sciencedirect.com/science/article/abs/pii/S0043135412003995
- LI, Wei, Xiao-Yu SHAN, Zhi-Yao WANG, et al. Effect of self-alkalization on nitrite accumulation in a high-rate denitrification system: Performance, microflora and enzymatic activities. Water Research [online]. 2016, 88, 758-765 [cit. 2020-10-20]. ISSN 00431354. Dostupné z: https://www.sciencedirect.com/science/article/abs/pii/S0043135415303316
- LAHDHIRI, Ameni, Geoffroy LESAGE, Ahmed HANNACHI a Marc HERAN. Minimum COD needs for denitrification: from biological models to experimental set-up. DESALINATION AND WATER TREATMENT [online]. 2017, 61, 326-334 [cit. 2020-09-23]. Dostupné z: https://www.deswater.com/home.php
- PAUL, Eldor Alvin. Soil Microbiology, Ecology and Biochemistry. 3rd Edit. Amsterdam: Elsevier, 2007. ISBN 978-0-12-546807-7.
- CAO, Duantao, Ruilin WU, Suxia DONG, et al. Triazole resistance in Aspergillus fumigatus in crop plant soil after tebuconazole applications. Environmental Pollution [online]. 2020, 266 [cit. 2020-10-19]. ISSN 02697491. Dostupné z: https://www.sciencedirect.com/science/article/abs/pii/S0269749120304218
Komentář k již recenzovanému vítěznému textu soutěže JUNIORSTAV: Znečištění povrchových a podzemních vod dusičnany je celosvětovým problémem a na evropské úrovni je řešeno v rámci směrnice Rady 91/676/EHS. Denitrifikační bioreaktory jsou účinnou metodou odstraňování dusičnanů z drenáží, poprvé byly testovány v roce 1994 ve Spojených státech. Technologie má perspektivu i v odstraňování patogenních mikroorganismů a mikrobiálního znečištění. V současné době jsou dostupné studie, které se zabývají i sledováním případného negativního vlivu náplně v bioreaktoru (směs štěpky z různého dřeva, bříza, smrk apod.) na ekosystém. Problematiku využití denitrifikačních bioreaktorů pro potřeby snížení koncentrace toxikantů, životnost zařízení, charakter náplní apod. dlouhodobě řeší výzkumné pracoviště firmy Dekonta, a.s. ve spolupráci např. s VŠCHT Praha, UK Praha, TU Brno atd.
Denitrifying bioreactors are used to remove nitrates from surface runoff in agricultural areas and thus to prevent them from entering surface water bodies. The course and rate of the denitrifying process is influenced by many factors. One of the most important ones is the inflow water quality, as the water can be contaminated also by pollutants such as pesticides.
We have paper proposed and optimized a methodology for the long-term testing of the effect of pesticides on the denitrification process. This batch test was performed to evaluate the inhibition of the denitrification rate. Apart from optimizing the nitrate dosage method, we determined as well their optimal dose (15 mg/l) and also the most suitable NaHCO3 concentration in the deionized water (0.5 mg/l).